水の硬度測定(キレート滴定) サブメニュー 原理 > 試薬・器具 > 操作 > 流れ図 > 実験プリント リンク < 項目メニューへ戻る・・・・・・ 酸化還元滴定用 (3) 銅、亜鉛 ・・・・・・ キレート滴定用 (4) 塩化ナトリウム、フッ化ナトリウム ・・・・・・ 沈殿滴定用 補記:三酸化二ヒ素はjis 「容量分析用標準物質」では削除されています。 いずれも室温で安定な固体であり、jis薬剤師国家試験 令和02年度 第105回 一般 理論問題 問 92 酢酸亜鉛は、ウィルソン病や低亜鉛血症の治療薬として用いられているが、副作用として銅欠乏症を生じる場合がある。亜鉛化合物の定量には一般にキレート滴定法が用いられる。日本薬局方におい

公開公報 特定成分に関するものに関する技術公報一覧 Astamuse
キレート滴定 計算 銅
キレート滴定 計算 銅-JPB2 JPA JPA JPB2 JP B2 JP B2 JP B2 JP A JP A JP A JP A JP A JP A JP B2 JP B2 JP B2 Authority JP Japan Prior art keywords concentration solution copper plating ion chelating agent Prior art date Legal statusEDTA と金属キレートのK f 値→p18, 表12 <例:EDTA とMg2> K f = 49×108 log K f = 8 log 49 = 869 ML n M Ln 8 キレート滴定 多座配位子EDTA(標準液)が 金属イオン(Zn 2, Mg 2, Ca , Al3, Cu 等)と 水溶液中で安定な可溶性のキレート化合物を生成する ことを利用した滴定法




Dviout 酸と塩 Pdf 無料ダウンロード
1週 工場見学 工場見学に行き,学んだことを報告できる。 2週 計画 結晶硫酸銅中の銅4.キレート滴定 41 001Medta標準溶液の調製 要点 キレート滴定において標準溶液として用いられるedtaは、普通edtaの2ナトリウム 塩h2na2y・2h2oでetaと表示されている。この試薬は結晶水以外に多少の水分を含んで いるので、通常は約80℃で数時間乾燥して使用するが、本実験では精密な分析キレート滴定における終点の検出 金属指示薬:金属イオンの濃度変化により鋭敏に変色 (指示薬も金属イオンとキレートを形成する) エリオクロムブラックt (ebt) n n oh oh so 3 h no 2 h3in 2 ph 変化に伴うebt 指示薬の色調変化 n n oh oh so 3 h no 2 h3in pka1=16 pka2=63 pka3=115 n n oh oh so3no2 h2inn n o oh so 3no
キレート滴定を理解し,濃度などの計算ができる。 器具の洗浄,確認,清掃を行うことができる。 16週 後期;測定手法 キレート滴定 関連規格 astm d 本アプリケーションノートではastm d に基づく、水中のカルシウムイオン、マグネシウ ムイオン濃度の測定例を紹介します。 水中のカルシウム、マグネシウム濃度の指標として水の硬度が用いられます。一般にカルシウ ム、マグネシウム濃度を4.キレート滴定 41 001Medta 標準溶液の調製 要点 キレート滴定において標準溶液として用いられる edta は、普通 edta の2ナトリウム 塩 h 2 na 2 y・2h 2 o で eta と表示されている。 この試薬は結晶水以外に多少の水分を含んで いるので、通常は約80℃で数時間乾燥して使用するが、本実験では精
過滴加 mL 1 mL 計算式 (DB)*K*F*M/S 最大滴加mL mL 小数点以下桁数 3 滴定液名 01mol/L EDTA 電極名 自動入力先パラメータ 無し 滴定条件例 滴定曲線例 測定結果 測定回数 試料量(mL) 滴定値(mL) 濃度(g/L) 1 5 7623 9639 2 7603 9614となる。 キレート滴定では、この至適 pH を保つために緩衝液が用いられる! XIII13 補助錯化剤 一般にキレート滴定はかなり高い pH で行なうが、このとき金属水酸化物を沈殿させな いように、 EDTA より Kf の小さい錯化剤(=補助錯化剤 )を共存させることがある ⇨⇨ マスキング実験操作 キレート滴定による銅水溶液の滴定 硫酸銅水溶液についてpH5~6でTARを指示薬としてEDTA標準溶液で滴定する。 約005mol l1硫酸銅水溶液を3個のコニカルビーカーに,ホールピペットを用いて2mlずつ採る。 メスシリンダーで純水約50mlを加え,さらに緩衝溶液2mlとTAR指示薬(01%



クレゾールフタレイン Wikipedia




キレート滴定
13キレート滴定(亜鉛(II)EDTA , 塩化銅(II)EDTA , のキレート滴定法を学ぶ) 11沈殿滴定(塩化ナトリウム硝酸銀溶液の試料をMohr法、Fajans法を用いての沈澱滴定) 広告 資料を推薦する 優良な資料があれば、ぜひ他のユーザーに推薦してください。資料詳細ページの資料右上にある推薦ボタンを · About Press Copyright Contact us Creators Advertise Developers Terms Privacy Policy & Safety How works Test new features Press Copyright Contact us Creatorsキレートメトリー(chelatometry),コンプレクソンメトリーともいう.水溶液中で金属イオンとキレート試薬とのキレート生成反応を利用して行う定量分析法で,終点の決定には金属指示薬,pH変化の測定,電位差法,光度法などがある.G Schwarzenbachらにより開発されたEDTA試薬による Ca 2+ ,Mg 2+ を滴定する方法は代表的なものである.




Edta キレート エチレンジアミン四酢酸 Edta




ミネラル サプリ キレート 滴定
· EDTA溶液の濃度(mol/l)×EDTA溶液の滴定値(ml)=Ca2とMg2の濃度の総和(mol/l)×試料量(ml) (式) × 3005 = x × 50 = 50x x = (mol/l) · 質問者: redbird13 質問日時: 0940 回答数: 1 件 約005Mの硫酸銅溶液を001MのEDTA・2Na標準溶液で滴定しました。 滴下量は993mlでした。 銅イオンのモル濃度を決定したいのですが、反応式がわからないため、計算がわかりません。 誰かわかる方お願いします。 通報する この質問への回答は締め切られました。京都大学 全学共通教育 基礎化学実験ホームページ:http//wwwchemzenkyohkyotouacjp/化学実験操作法:操作法 2 4 キレート




キレート滴定 銅の定量 Youtube




7798 23 4 りん酸銅 Ii Copper Ii Phosphate 032 043 036 詳細情報 試薬 富士フイルム和光純薬
方法が広く用いられている。これをキレート滴定という(参考(1)参照)。ここでは水の硬度測定すなわちCa2,Mg2の濃度を キレート滴定によって定量する方法を理解する2)。 < 要 点 > 硬度とは水中のCa2およびMg2の量をCaCO 3(mg CaCO3/L)に換算したものである。硬度には全硬度級),硝酸銅(悶)三水和物(国産化学 KK ,試薬特級) )イオンの場合生成熱が小さいが比較的誤差は小さい。この温度滴定の計算上の終 点は, NiINHが1 1 5である。これは銅イオンのところで触れたようにINHがキレート化 するときに配位している水と置換する過程でChart1の( a)の状態るphn銅 錯体の生成定数k=50×109が 得られたedtaに より銅(ii)を キレート滴定するとき, PHNを 指示薬とした場合,当 量点付近の変色は赤とう色から淡青色になった点であるこ れを光度滴




キレート滴定法の意味 用法を知る Astamuse
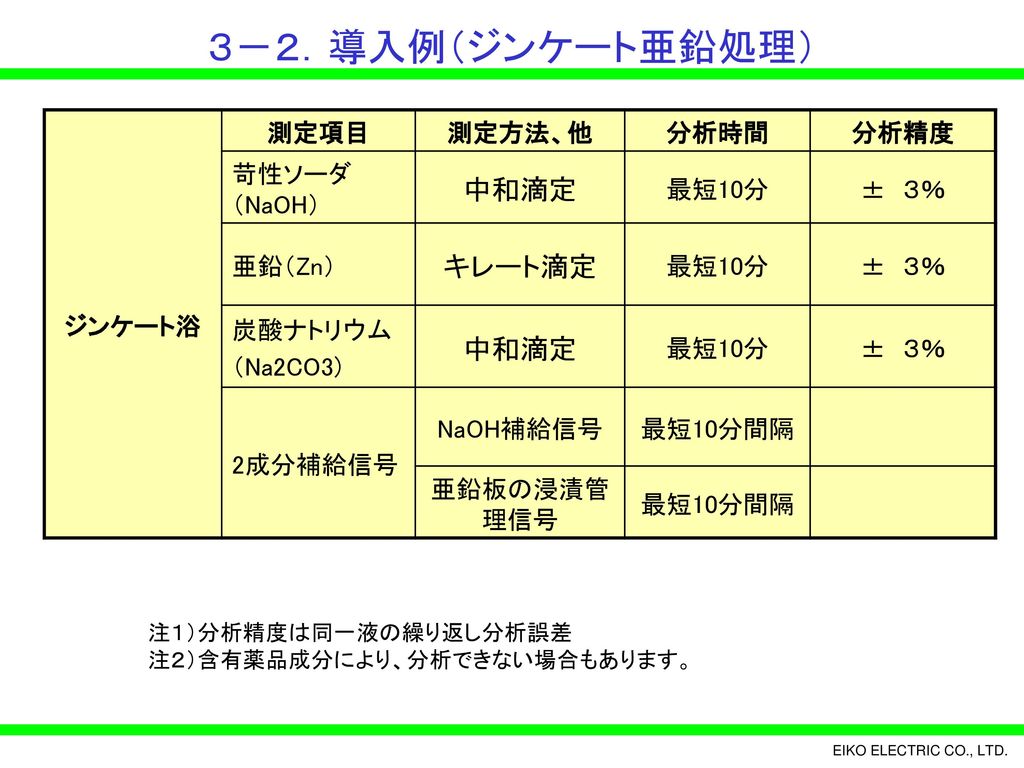



薬液処理浴自動管理装置 めっき管理主任シリーズ のご紹介 Ppt Download
容量分析(キレート滴定によるCaの定量) <容量分析とはどのような分析法か> 酸-塩基の中和反応を例として、容量分析の原理を説明する 01mol/lのHClをビューレットにいれる 三角フラスコの中に、総量0001 mol となるよう、NaOH水溶液を入れる ex(01 mol/l のNaOH水溶液を( ) ml 分取すれば用いてEDTA 滴定液によって光度滴定した例を紹介します。 Zn2+ + Na 2 EDTA → ZnEDTA + 2Na + 2.装置構成および試薬 (1)装置構成 本体 : 平沼自動滴定装置 COM シリーズ(光度滴定用測定ユニット Mタイプ) 使用フィルタ 530nm (2)試薬工学基礎化学実験 容量分析≪キレート滴定法、酸化還元滴定法による銅の定量≫ 実験目的 キレート滴定とは、多座配位子であるエチレンジアミン四酢酸(EDTA)のようなキレート試薬を用いる一種の錯滴定であり、酸化還元滴定とは、過マンガン酸塩、二クロム酸塩、チオ硫酸塩のような酸化
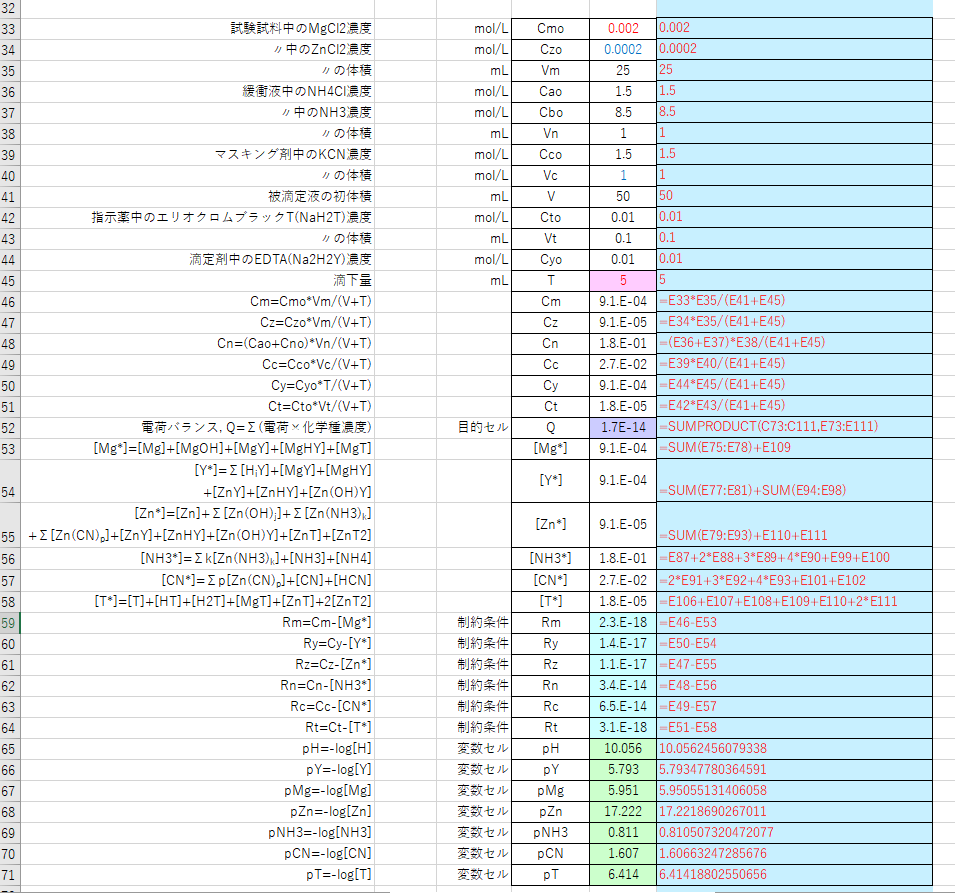



Edta滴定における妨害金属イオンのマスキング 滴定曲線 溶解度などーエクセルを用いて
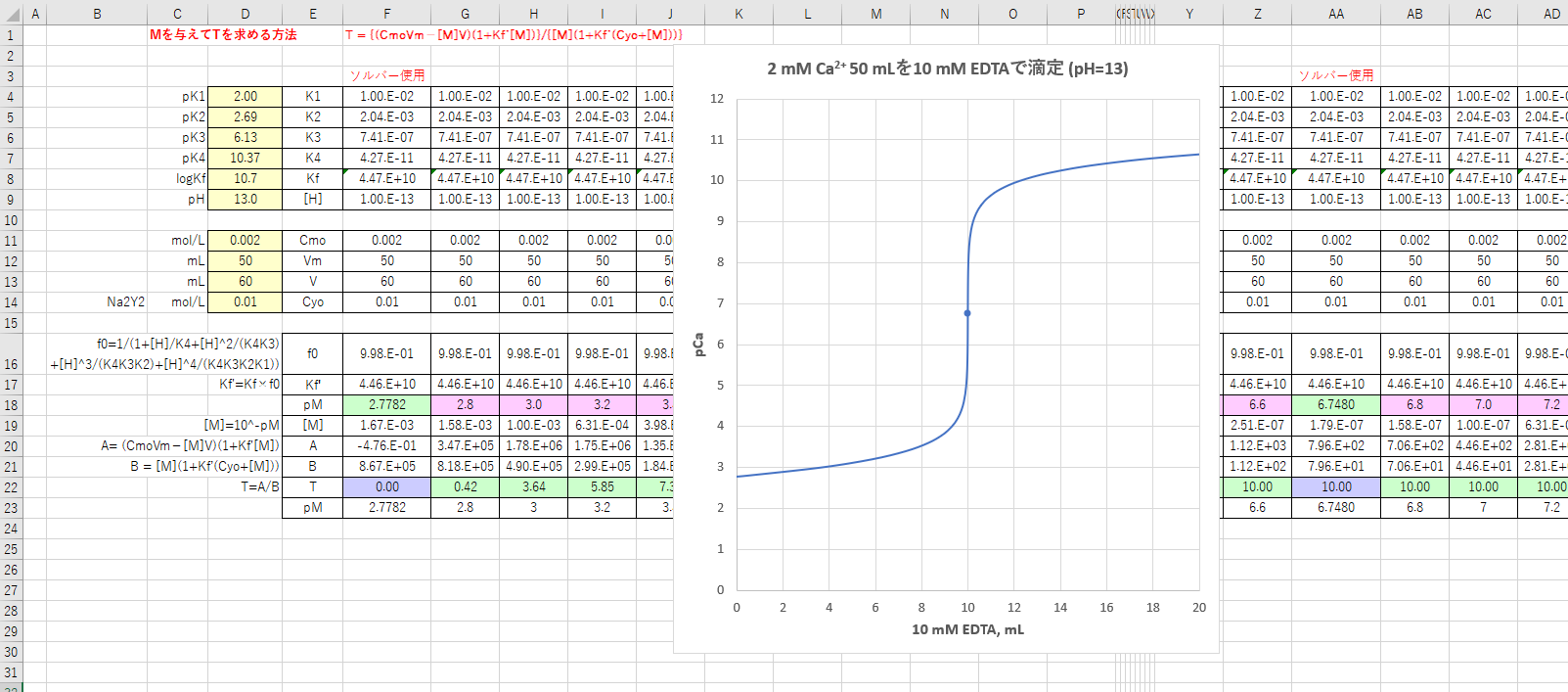



カルシウムのedta滴定 1 滴定曲線 溶解度などーエクセルを用いて
二ナトリウム塩 (na 2 h 2 edta ) 溶液を用いた キレート滴定 により分析する。これらの金 属は edta との錯体の安定度定数が近いので、 cu 2 イオンはマスキング剤(チオ硫酸 塩)によってマスキングする。最初に銅と亜鉛を、 edta によって一緒に滴定する。次 · 銅を含む標準資料があり、水に溶かして溶液として、キレート滴定をおこなった。 銅の原子量は6355である。 標準試料を0ml水溶液にしてそのうちのmlを使って滴定をおこなった。 用いたEDTA用液の濃度は005Mである。 結果、標準質量はgで適定量は1463mlであった。 銅の含有量(wt%)を求めよ 計算過程を教えて欲しいです、お願いします 化学 数学 ・ 77 閲覧キレート滴定 (chelatometric titration)などの錯化滴定*1 においては,金属イオンMn は ルイス酸であり,配位子はルイス塩基である。キレート滴定曲線は,滴定剤 (ルイス塩基)の添加量に対して,pM(= log Mn)の値を縦軸にとって 表示する。



64 7 ジ M ヒドロキソビス N N N N テトラメチルエチレンジアミン 銅 Ii 二塩化物 Di Mu Hydroxo Bis N N N N Tetramethylethylenediamine Copper Ii Dichloride 327 323 詳細情報 試薬 富士フイルム和光純薬




Dviout 酸と塩 Pdf 無料ダウンロード
キレート滴定の手法は、「銅及び銅合金中のニッケル定量方法」jis h 1056 を参照し、一定量の edta を加えてニッケルの edta 錯体を生成させた後、過剰の edta を亜鉛の溶液で滴定するという、逆滴定を採用しました。 ただし亜鉛の標準溶液を作るのが手間なので、市販の edta ナトリウム塩が純品でキレート滴定の原理図拡大 pH12~13において、Mg 2+ は安定な水酸化物となってEDTAと反応しなくなるので、このpH領域で作用するNN指示薬を用いて Ca 2+ のみを定量することができる。 試料水中に含まれる、Fe 2+ 、Cu 2+ などもEDTAと反応するが、隠ぺい剤としてNa2Sを加えておくと、 · キレート滴定(キレートてきてい)とは。意味や解説、類語。金属イオンなどの試料物質が、適当な配位子と反応してキレート化合物を作ることを利用した滴定法。 goo国語辞書は30万4千件語以上を収録。政治・経済・医学・ITなど、最新用語の追加も定期的に行っています。




07 号 キレート剤の測定方法およびキレート剤の測定キット Astamuse
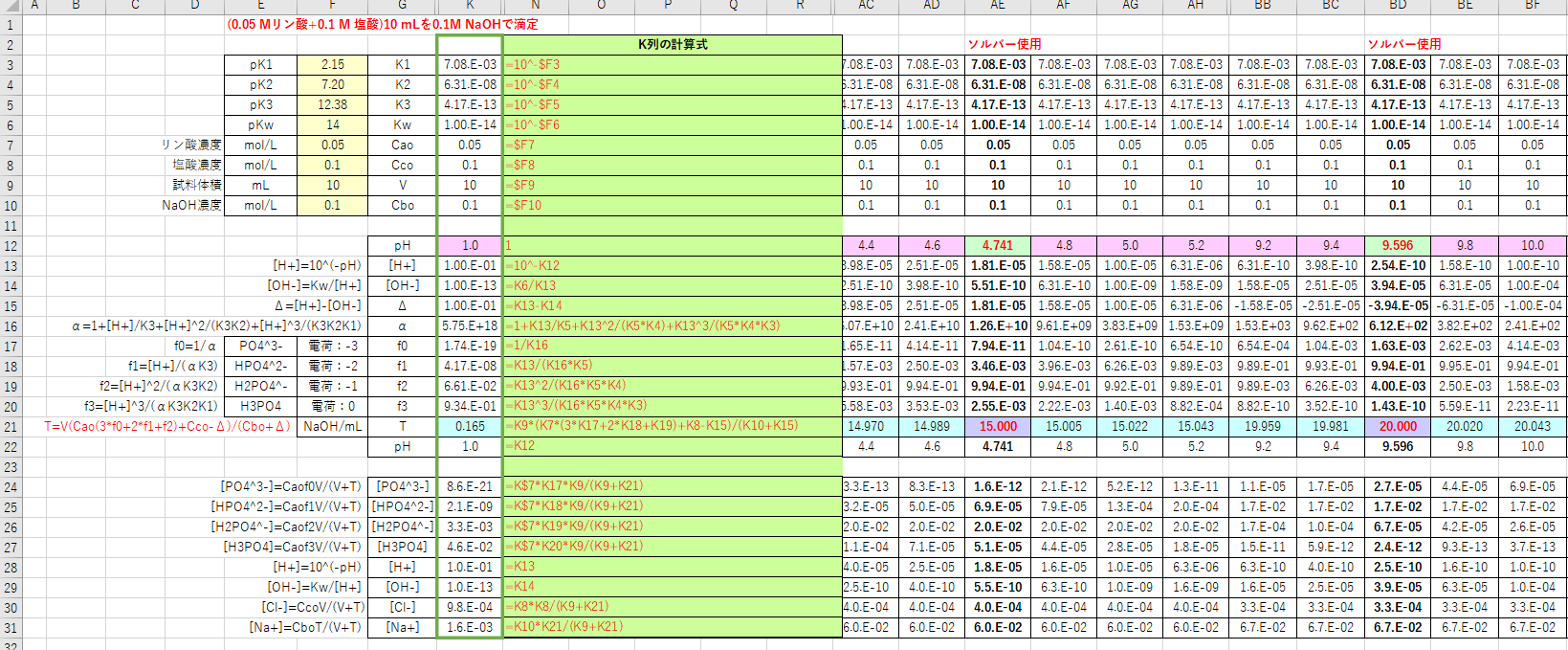



滴定曲線 滴定曲線 溶解度などーエクセルを用いて
キレート滴定の計算方法 1 試薬の体積と初濃度 塩化アンモニウムNH 4 Cl-アンモニア水NH 3 系のpH緩衝液により,常にpH=10一定であると仮定する.計算を簡単化するために,カルシウムイオンCa 2 やマグネシウムイオンMg 2 と指示薬のエリオクロムブラックT(EBT)の錯体形成反応(化学平1 EDTA とは 近年,分 析化学に関する研究鞭告や,JISの 試験法に EDTAま たはエチレンジアミン四酢酸という試薬の名 前,あ るいはキレート滴定法という言葉がよく出てくる ことに気がつかれた読者が多いことと思います EDTA とは,つ ぎに示すような構造の有機化合物で,英 語で ethylendiaminetetraacetic acidと 呼ぶので,こ れを 省略してEDTA,あ るいは日本語でエチレンジア · キレート滴定 要旨 まず亜鉛の固体を精秤しこれを酸で溶かす。この亜鉛溶液でedtaを標定し、そのedtaで塩化銅(ii)を標定する。 目的 金属イオンを容量滴定によって標定する方法としては、エチレンジアミン四酢酸(edat)によるキレート滴定が最も一般的である。




17 号 可搬型滴定装置 Astamuse




キレート滴定 Kyo Aroma Breath 京都 京北での精油採取から 暮らしの香りへ
キレート滴定 1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。また、実験を通してキレート滴定法 の原理や操作の仕方について学び、結果の考察をしてさらに理解を深める。 2.原理 金属イオンに配位し、キレート化合物を形成する多座配位子をキレート試薬と呼ぶ。こ*「キレート滴定」上野景平著(南江堂出版)より Q Tiの逆滴定 A この方法は逆滴定になります。下記方法を参考にして下さい。 <試薬> ・001mol/L EDTA標準液 ・001mol/L CuSO 4 標準液 ・PAN指示薬溶液 ・50% NaOH溶液 ・30% H 2 O 2 溶液 <操作> ①Tiを含む試料を硫酸白煙まで加熱したのち、室温 · 1 回答 キレート滴定の問題です。 キレート滴定の問題です。 0010Mの銅 (Ⅱ)イオンと0010MのEDTAを含むpH400の溶液において、フリーの銅 (Ⅱ)イオンは銅全濃度の何パーセントを占めるか。 ただし、CuY2の生成定数は63×10^18であり、pH400におけるα4=33×10^ (9)とする。 これを解いてください。
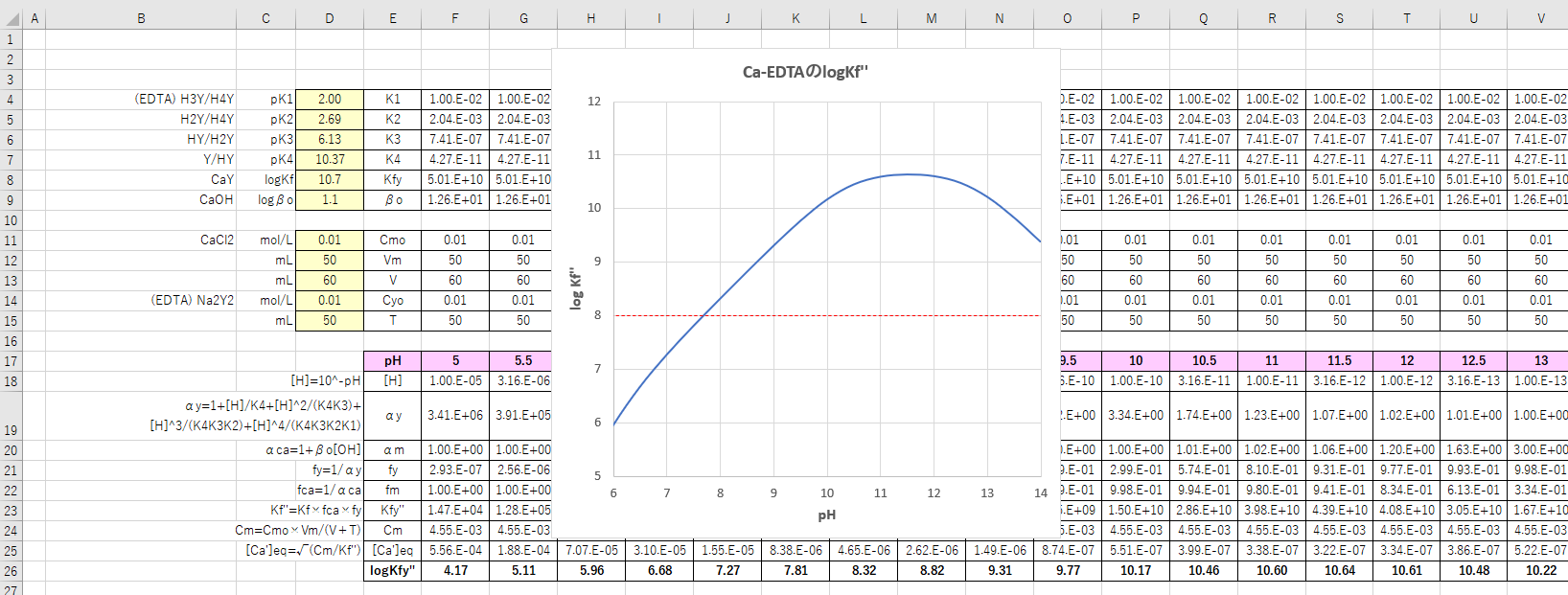



カルシウム 滴定曲線 溶解度などーエクセルを用いて




キレート滴定 Kyo Aroma Breath 京都 京北での精油採取から 暮らしの香りへ




Edta キレート エチレンジアミン四酢酸 Edta




塩基性硫酸銅 Ii Copper Ii Sulfate Basic 037 031 詳細情報 試薬 富士フイルム和光純薬




キレート滴定



質問箱



水の硬度 株式会社ユニケミー ユニラボ



メタロアッセイ 低濃度銅測定 Ls 尿中銅定量キット Metallogenics



3回生実験のこと 合金の分析




Woa1 吸水性樹脂の製造方法 Google Patents




Woa1 血液分析方法及び血液検査キット Google Patents




キレート滴定 Kyo Aroma Breath 京都 京北での精油採取から 暮らしの香りへ




キレート滴定




活性化液 カドミウム 銅充填カラム用 Activating Solution For Cd Cu Packed Column 016 詳細情報 試薬 富士フイルム和光純薬



公開特許公報
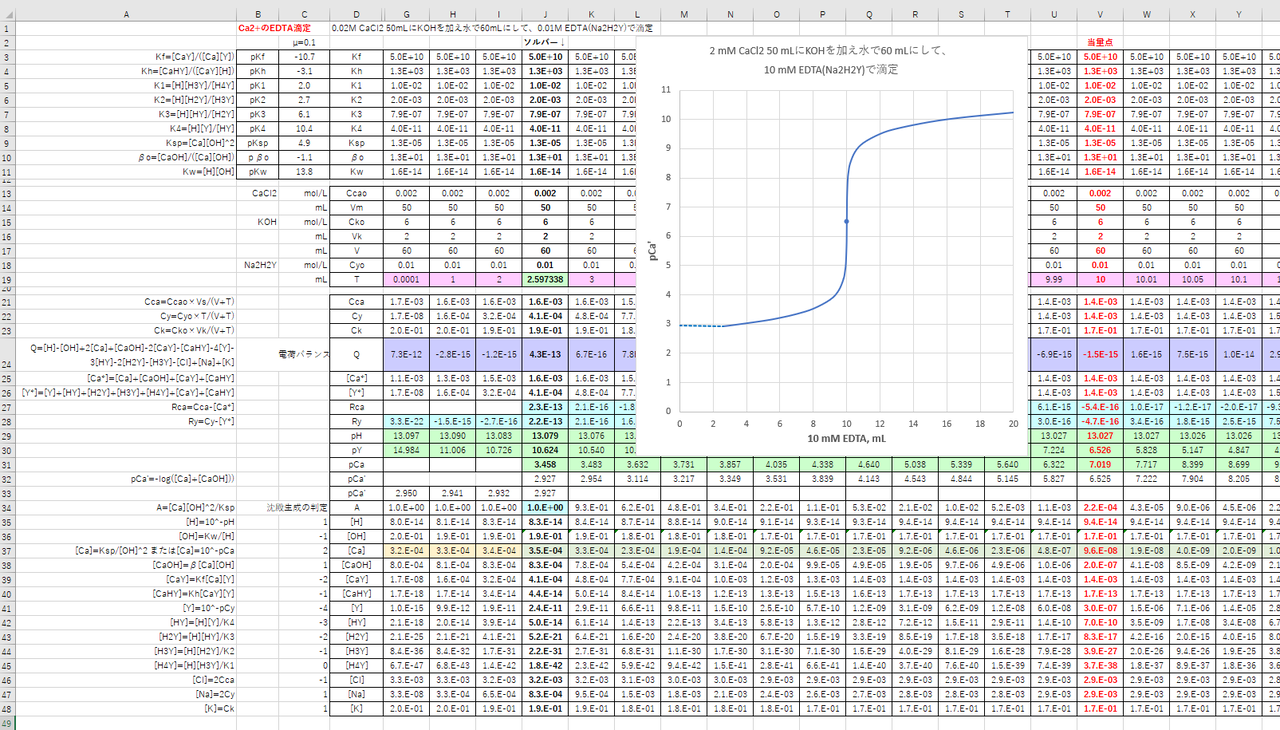



カルシウムのedta滴定 1 滴定曲線 溶解度などーエクセルを用いて




公開公報 特定成分に関するものに関する技術公報一覧 Astamuse




17 号 可搬型滴定装置 Astamuse
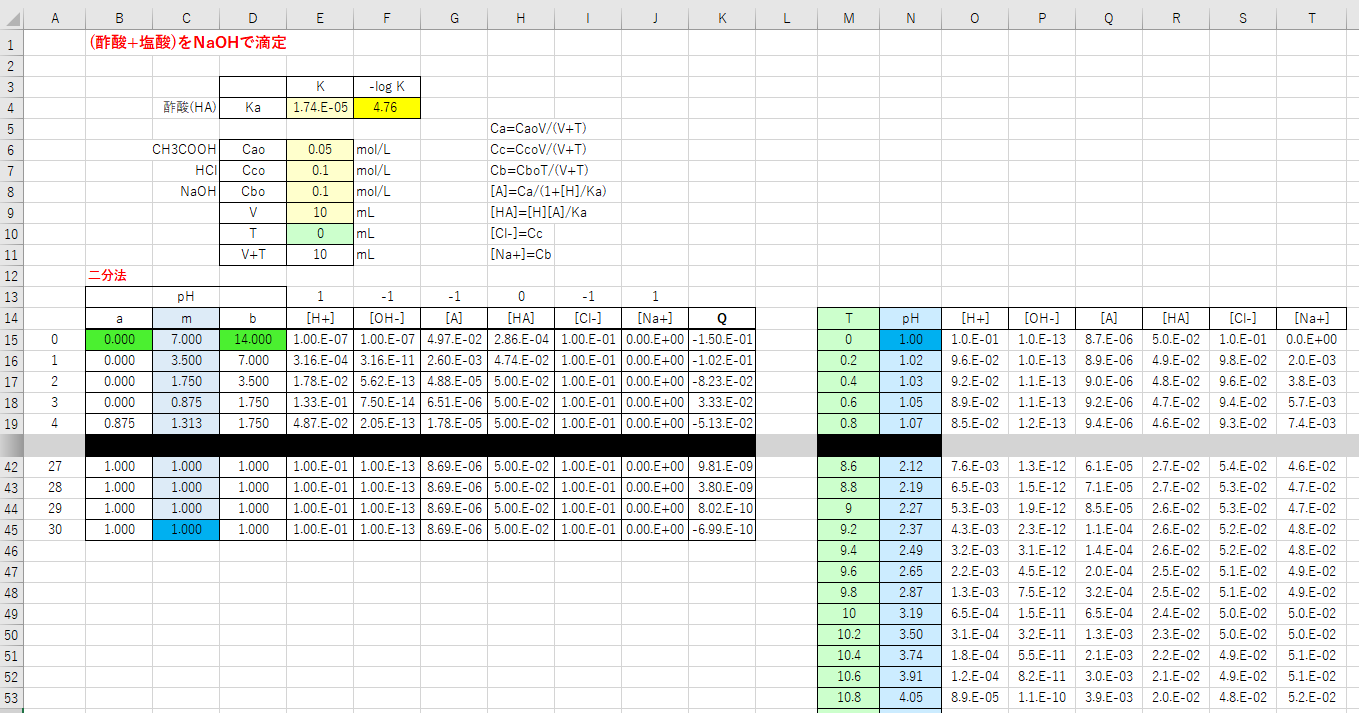



滴定曲線 滴定曲線 溶解度などーエクセルを用いて




塩基性炭酸銅 Ii Copper Ii Carbonate Basic 035 039 詳細情報 試薬 富士フイルム和光純薬




Edta滴定における妨害金属イオンのマスキング 滴定曲線 溶解度などーエクセルを用いて



3回生実験のこと 合金の分析




国際化学オリンピックに挑戦 5 実験 国際化学オリンピックobog会 本 通販 Amazon




17 号 可搬型滴定装置 Astamuse




The Chemioal Chemical Society Sooiety Of Japan 生成反応がすすむため 沈殿は Cu Nh3 4p を作り つつ溶解する このため濃度の大きい場合ほど その頂 とが確認でき 錯体化学における当量関係を理解させ 一助とすることができた 点勾 Pdf Free Download




キレート生成反応 1 検査と技術 2巻8号 医書 Jp




17 号 可搬型滴定装置 Astamuse
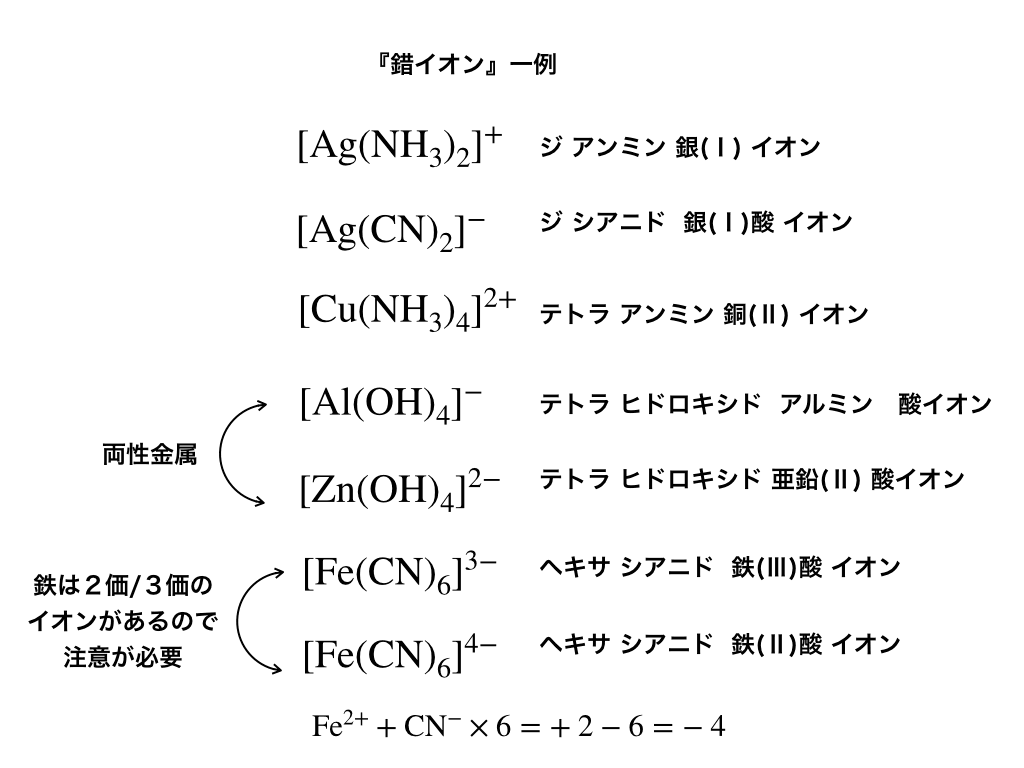



錯イオンとは 命名法や構造 配位子などの意味 覚え方まで詳しく解説



0 件のコメント:
コメントを投稿